마약류에 대한 관리가 기존 ‘기록·보관의무’에서 ‘취급내역 전산보고’ 조항으로 확 바뀐다.
수면마취제인 프로포폴을 피로회복주사로 투약하는 등 의료용 마약류에 대한 오·남용이 사회 문제로 부각되면서 엄격한 관리 필요성에 대한 국민적 공감대가 형성된데 따른 것이다
이에 따라 2018년 5월 18일부터 마약류 제조업체, 수·출입업체, 도매상, 병·의원, 약국, 학술연구자 등 마약류취급자와 공무상 마약류사용자 등 마약류취급승인자는 수입·수출, 제조·사용, 판매·구입, 조제·투약, 양도·양수, 폐기 등 모든 취급내역을 마약류통합관리시스템으로 전산보고 한다.
관리시스템이 정착되면 의료용 마약류에 대한 국가적인 모니터링 체계를 구축하는 것은 물론 피로회복주사(수면마취제), 공부 잘하는 약(각성제), 살 빼는 약(식욕억제) 등 그릇된 약물 사용과 과다처방 및 의료쇼핑 등 약물 남용을 억제하여 국민건강을 보다 적극적이고 예방적으로 보호할 것으로 기대되고 있다.
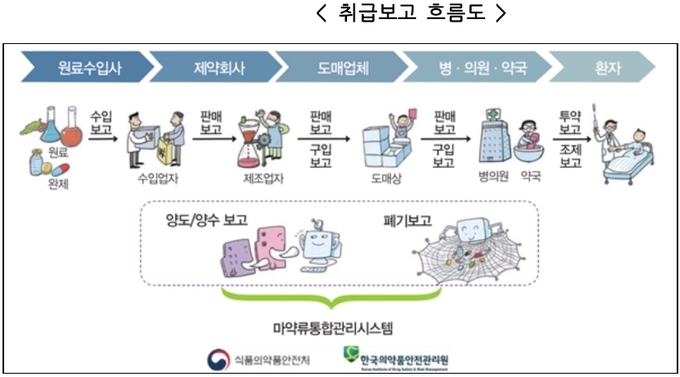
식품의약품안전처(처장 류영진)는 마약류취급자 및 마약류취급승인자가 마약류 제조‧수입‧유통‧사용 등 모든 취급 내역을 ‘마약류통합관리시스템’을 통해 보고하는 ‘마약류 취급보고 제도’를 5월 18일부터 본격 시행한다고 밝혔다.
이번 제도 시행은 마약류 취급의 모든 단계를 상시 모니터링하여 그 동안 발생했던 펜타닐, 프로포폴 등 마약류의 오남용과 불법 유출 사례를 예방함으로써 촘촘한 마약류 안전관리망을 구축하기 위한 것이다.
마약류 취급보고 제도의 주요 내용은 ▲‘마약류통합관리시스템’을 통한 취급내역 보고 ▲의료용 마약 및 향정신성의약품을 ‘중점관리품목’과 ‘일반관리품목’으로 구분‧관리 등이다.
모든 마약류취급(승인)자는 제도 시행 이전에 보유하고 있던 마약류 재고정보를 마약류통합관리시스템에 등록하여야 한다.
다만, 마약류취급의료업자(병·의원)와 마약류소매업자(약국)는 의료현장에서 진료에 차질이 발생하지 않도록 하기 위하여 5월 17일 이전에 구입하여 사용하고 있는 마약류에 대해서는 기존 ‘마약류관리대장’으로 작성하면서 우선 소진할 수 있다.
이 경우 해당 관리대장 기록은 2년 동안 보관해야 하며, 5월 18일부터 구입한 마약류는 시스템을 통해 취급내역을 보고해야 한다.
마약류는 ‘의약품 일련번호’ 정보를 기반으로 추적할 수 있는 ‘중점관리품목’ 마약류와 ‘제조번호별 수량’ 정보를 기반으로 하는 ‘일반관리품목’ 마약류로 구분‧관리한다.
마약과 프로포폴은 ‘중점관리품목’으로 모든 취급내역을 취급한 날로부터 7일 이내에 보고해야 하며, 프로포폴 외 향정신성의약품은 ‘일반관리품목’으로 취급한 달의 다음달 10일까지 마약류통합관리시스템으로 보고해야 한다.
식약처는 새롭고 엄격한 의무보고 제도가 시행됨에 따라 보고자가 시스템에 적응하는데 도움을 주기 위하여 전산보고의 단순 실수나 착오 등에 대해서는 행정처분을 유예하는 계도기간을 운영한다.
행정처분 유예 대상은 ▲단순 실수로 마약류 취급내역을 잘못 입력하는 경우(`18.12월) ▲보고 과정에서 일부 누락하거나 착오로 잘못 보고한 경우(`18.12월) ▲시스템 오류로 미보고한 경우(`18.12월) ▲마약, 프로포폴과 같은 ‘중점관리품목’의 ‘일련번호’ 입력 실수한 경우(`19.6월) ▲병의원‧약국에서 조제‧투약보고 시 ‘중점관리품목’의 ‘일련번호‧제조번호‧사용기한’ 입력 실수나 미입력의 경우(`19.6월) 등이다.
마약류의 모든 취급내역을 보고하지 않아 관할 행정기관이 1차 계도(시정)하였음에도 계속해서 보고하지 않은 경우와 마약류 취급내역을 허위‧조작하여 거짓으로 보고하는 경우에는 행정처분을 받는다.













