식품의약품안전처(처장 류영진)는 식품첨가물 신규지정 시 제출하는 안전성 자료 중 최종제품에 남지 않는 가공보조제와 소량 사용‧섭취하는 향료에 대해서 반복투여독성 및 유전독성 자료만 제출하도록 개선하는「식품첨가물의 기준 및 규격」고시 개정안을 9월 28일 행정예고 한다고 밝혔다.
개정안 주요 내용은 ▲가공보조제 등 신규지정 시 제출자료 범위 개선 ▲β-카로틴 제조가능 범위 확대 ▲α-아밀라아제 생산가능 균주 추가 신설 등이다.
식약처는 앞으로도 식품의 안전성 확보와 식품산업의 활성화를 위해 식품첨가물 기준·규격을 합리적으로 개선할 계획이라고 밝혔다.
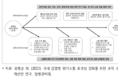
1. 가공보조제 등 신규지정 시 안전성 제출자료 범위 개선
품 목 명 | 개 정 내 용 |
가공보조제 향료 | ○ 최종제품 완성 전 제거되거나 섭취가능성이 낮은 가공보조제 및 향료의 특성을 감안하여 안전성 제출 자료의 범위 완화 |
(현행) 모든 첨가물 | | (개정) 가공보조제, 향료의 경우 |
반복투여독성, 유전독성, 생식·발생독성, 면역독성, 만성·발암성시험 | 반복투여독성, 유전독성 * 다만, 안전성에 우려가 있을시 추가자료 제출 |
2. β-카로틴의 제조 가능 범위 확대
적용 대상 | 개 정 내 용 |
β-카로틴 | ○ Blakeslea trispora로부터 제조된 β-카로틴을 현행 “β-카로틴” 품목에 추가하고 정의 및 잔류용매 규격 추가·신설 |
3. α-아밀라아제의 생산가능 균주 추가 신설
품 목 명 | 개 정 내 용 |
α-아밀라아제 | ○ 기존 α-아밀라아제 정의에 생산 가능균주로 안전성이 확인된 유전자변형미생물 Aspergillus niger 추가 |