국내 제약산업이 글로화되는 길목에서 또다른 희망이 날아왔다.
의약품 GMP의 국제기준을 수립 및 주도하는 유일한 국제 협의체인 의약품실사상호협력기구(Pharmaceutical Inspection Co-operation Scheme, PIC/S)에 2014년 가입한데 이어 어제 'EU 화이트리스트 등재'가 확정 발표됐다.
화이트리스트 등재는 의약품실사상호협력기구(PIC/S)에 이어 다시 한 번 우리나라 제약 산업의 글로벌 시장 진출의 기폭제가 될 전망이다.
EU 화이트리스트 등재는 지난 2015년 1월 식약처가 신청서 제출 이후 약 4년을 넘겨 성사된 것으로 그동안 관계기관의 적극적인 노력 없이는 불가능 했다는 해석도 나오고 있다.
실제 식약처는 신청서 제출 이후 전담 대응팀을 구성하고 이를 중심으로 4년여 간 치밀하게 현장평가와 평가단 면담 등 심사절차에 대응한 것으로 전해지고 있다.
ㅡ국가별 의약품 수출현황
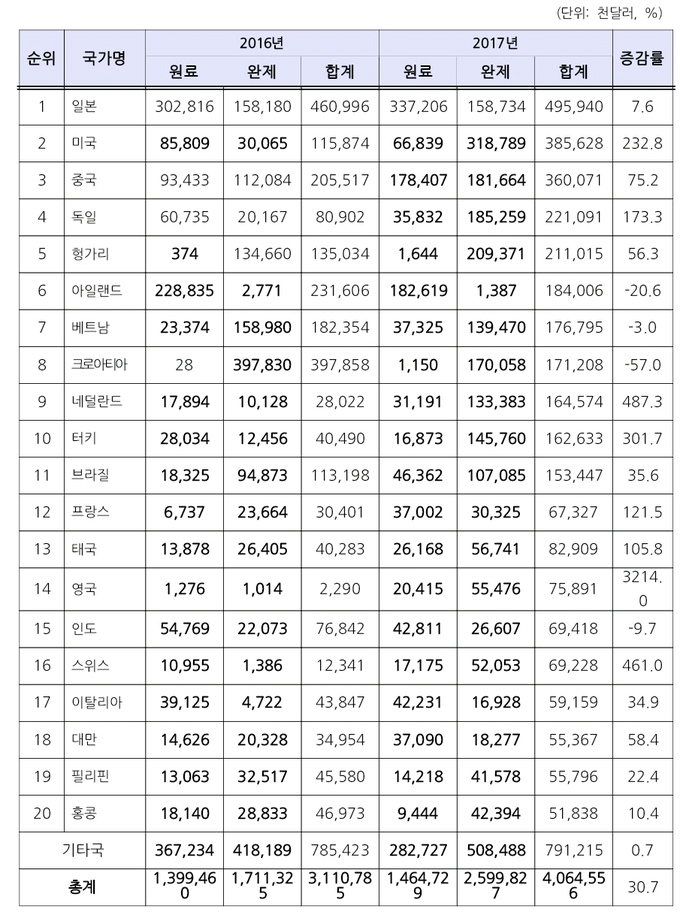
EU 화이트리스트란 유럽으로 원료의약품을 수출하고자 하는 국가에 대해 제조·품질관리기준(GMP) 운영 현황을 직접 평가하여 EU와 동등한 수준으로 인정되는 경우 원료의약품 수출 시 요구하던 GMP 서면확인서를 면제해 주는 것을 의미한다.
특히 이번에 우리나라가 등재된 것은 국내 원료의약품 GMP 운영체계나 국내 제약사의 원료의약품 품질이 EU뿐 아니라 미국, 일본 등 제약 선진국과도 동등한 수준임을 전 세계적으로 인정받은 것으로,EU에 수출하는 원료의약품의 경우, 국내 제약사는 GMP 서면확인서 면제로 수출을 위한 소요시간이 약 4개월 이상 단축되는 효과도 거둘수 있게 됐다.화이트리스트 등재국가는 스위스, 호주, 일본, 미국, 이스라엘, 브라질 총 6개국 (2019년 4월 현재, 등재순) 정도이다.
이에따라 미국 다음으로 의약품 시장규모가 크고 국내 의약품 수출액의 31%를 차지하고 있는 EU를 중심으로 수출이 확대되고 관련 산업이 성장할 것으로 예상된다.
EU의 경우 의료보장비용 절감 등을 이유로 제네릭 의약품을 확대하는 상황에서, 국내 제약산업에서 높은 비중을 차지하는 제네릭 의약품의 원료의약품 생산 업체에 수출 확대의 호재가 될 전망이다.
장기적으로는 제네릭 의약품을 중심으로 시장이 형성되어 있는 러시아 등 독립국가연합(CIS)이나 최근 의약품 분야 국가 간 협력이 강화되고 있는 베트남 등 아세안 시장으로의 활발한 진출도 기대된다.
한편 식품의약품안전처(처장 이의경)는 5월 14일(현지시각) 벨기에 브뤼셀에서 유럽연합(EU)이 이사회를 열고 우리나라를 7번째로 EU 화이트리스트(GMP 서면확인서 면제 국가)에 등재하였다고 밝혔다.













