식품의약품안전처(처장 오유경)는 ㈜셀리드사(社)가 신청한 국내 개발 코로나19 오미크론 백신 ‘AdCLD-CoV19-1 OMI’의 1·2상 임상시험계획을 8월 4일 승인했다고 밝혔다. 이로써 국내 개발 코로나19 관련 임상시험을 허가 받은 품목(상세 내용 아래 표 참조)은 10개로 늘어났다.
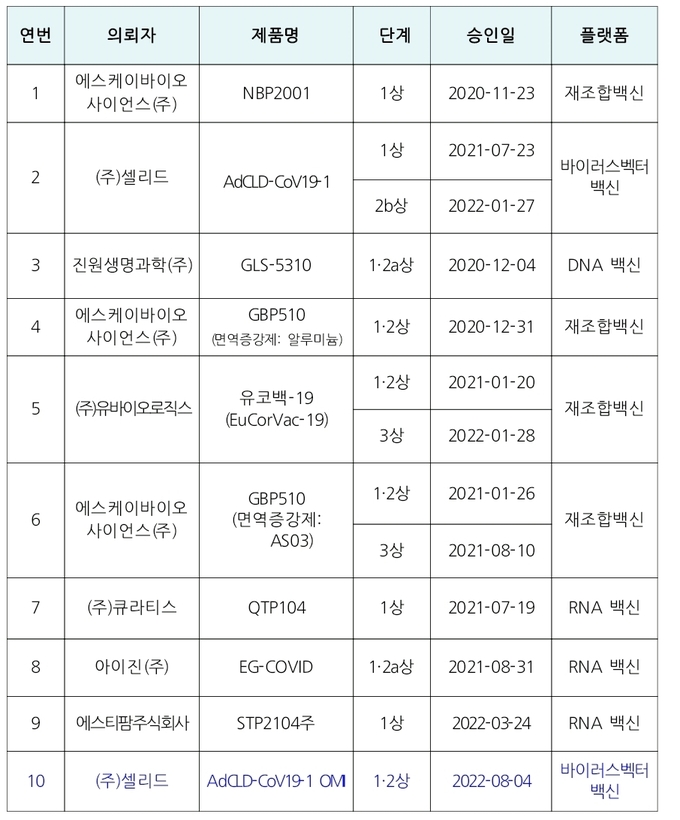
- 코로나19 임상시험 진행 현황(’22.8.04, 승인일 기준)
‘AdCLD-CoV19-1 OMI’는 코로나19 오미크론 변이 바이러스의 ‘표면항원 유전자’를 아데노바이러스 주형에 넣어 제조한 ‘바이러스벡터 백신’이며, 1·2상 임상에서는 안전성과 면역원성을 평가한다.
임상시험의 투여방법은 허가 백신 접종을 완료한 사람 또는 코로나19 확진 후 격리 해제된 사람에게 추가접종 형태로 1회 투여한다.