식품의약품안전처(처장 오유경)는 12월 27일 국제규격 등에 따라 안전성이 확보된 5개 의료기기 원재료와 10개 품목을 「의료기기 생물학적 안전성시험 면제 대상」에 추가하여 공고했다고 밝혔다.
인체에 직접 접촉하거나 삽입되는 의료기기는 허가 신청 시 생물학적 안전성시험 자료를 제출해야 하나, 국내‧외 규격 등에 따라 안전성이 인정되어 식약처장이 공고하는 원재료 및 품목은 자료를 제출하지 않아도 된다.
-생물학적 안전성시험 자료 제출 면제 대상
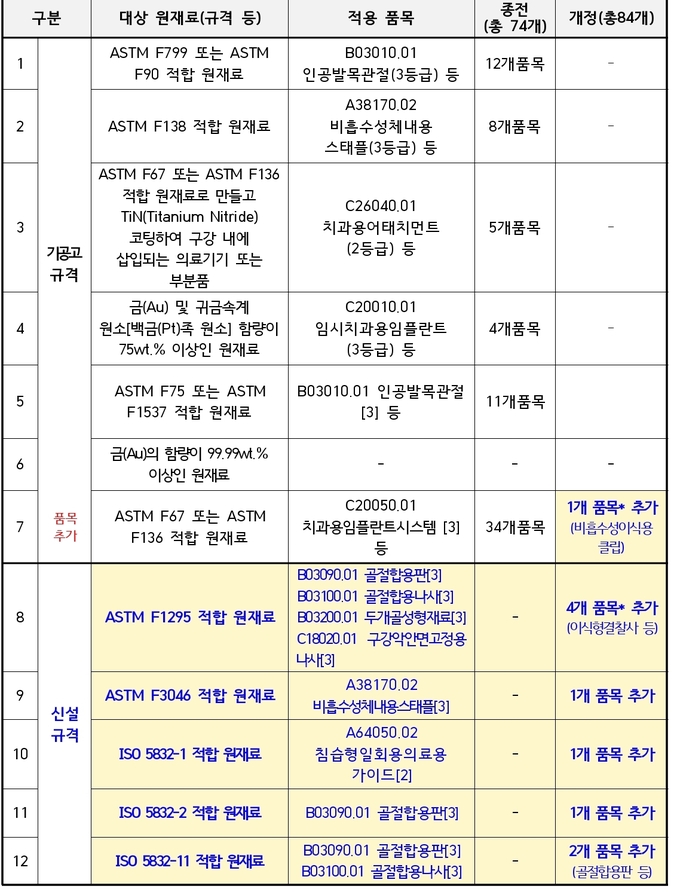
식약처는 국제적으로 생물학적 안전성이 인정된 원재료와 품목을 검토하여 충분한 근거가 인정되는 경우에 한해 면제 대상을 공고하고 있다. 이번 공고에서는 ASTM, ISO 등 국제규격에서 정한 원재료 및 품목 중 국내 허가 등으로 생물학적 안전성이 확인된 5개 원재료(티타늄합금, 스테인레스스틸 등)와 10개 품목(골절합용판, 골절합용나사, 두개골성형재료 등)를 추가하여 총 84개 품목으로 확대했다.
