신약 허가 받기가 어렵다는 것은 모두가 아는 사실이다. 하지만 이미 다른 제약사가 개발해 일정기간 판매하고. 있는 이른바 제네릭의약품의 개발도 결코 쉽지 않은 것으로 나타났다.
식약처에 따르면 제네릭의약품 품질심사 시 보완 없이 적합 판정 받은 품목이 32.2%, 1차 보완 후 적합 판정 품목이 48.1%, 2차 보완 후 적합 판정 품목이 19.7%로 확인되었다. 보완율은 총 2,792 품목 중 1,892 품목이 보완요청(67.8%)을 한 셈이다.
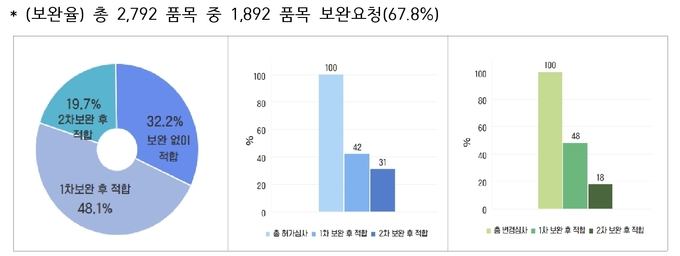
완제의약품 주요 보완 요청사항은 ➊제조방법 관련 자료(27.4%), ➋기준 설정 등 품질관리(24.8%), ➌개발경위(20.4%) 순이었다. 제조방법 관련 자료의 경우 「의약품의 품목허가·신고·심사 규정」개정*에 따라 제조방법에 대한 허가 후 변경관리가 강화되었기 때문으로 파악되고 있다.
원료의약품 주요 보완 요청사항은 ➊제조방법 관련 자료(33.1%), ➋분해생성물 특성 등 불순물에 대한 자료(22.2%), ➌품질관리 규격 기준 설정 자료(20.2%) 순이었다. 특히 불순물 관련 보완 중 유전독성물질에 대한 보완요청이 37.4%로 나타났다.
한편 식품의약품안전처 소속(처장 오유경) 소속 식품의약품안전평가원(원장 강석연)은 제네릭의약품 품질심사 시 개발사의 시행착오를 줄이고 심사 예측성을 높여 신속한 개발을 지원하기 위한 ‘제네릭의약품 품질심사 주요 보완사례집’을 10월 31일 발간한다고 밝혔다.
이번 사례집에서는 2023년 1월부터 2024년 6월까지 심사한 제네릭의약품 보완 요청사항을 분석한 결과를 제시하였다. 특히 업계가 품질 심사자료를 준비하는데 활용할 수 있도록 품질심사 시 자주 발생하는 주요 보완사항에 대해 보완요청 사유와 제출 자료 요건, 관련 규정 및 가이드라인을 상세하게 설명하였다.















