지난 11월까지 식약처의 품목허가를 받은 의약품과 의약외품은 모두246개 품목이며,신약은 72개,자료제출의약품은137개,안전성유효성 심사대상은 37개로 집계됐다.
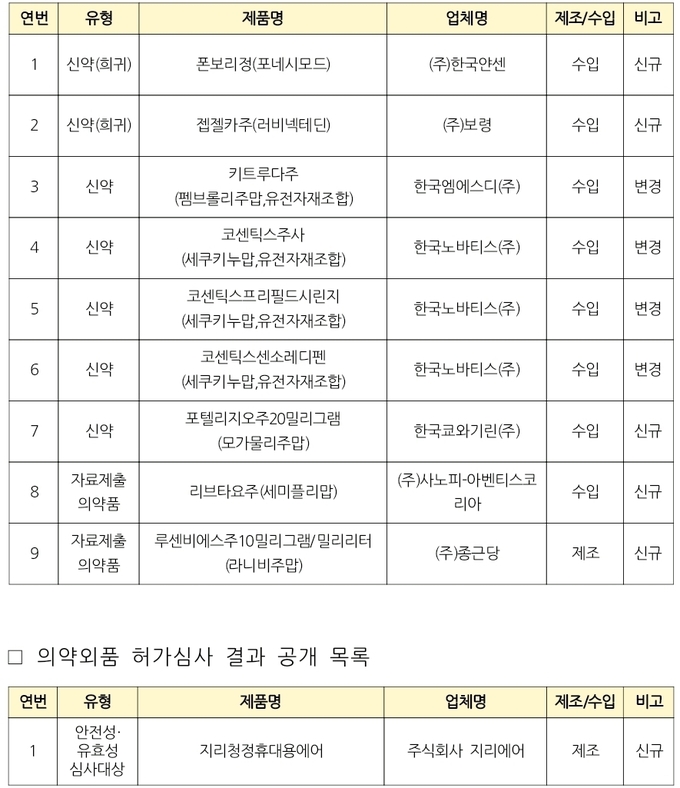
식품의약품안전처(처장 오유경)는 의약품과 의약외품 허가심사에 대한 투명성, 일관성, 신뢰성을 강화하기 위해 이같은 현황을 담아 지난 11월에 의약품 9개, 의약외품 1개 총 10개 품목(신규허가 6개, 변경허가 4개)의 허가심사 결과(허가보고서)를 공개했다.

이번에 공개된 대표적인 의약품은 ▲피부 T-세포 림프종 치료 신약 ‘포텔리지오주20밀리그램(모가물리주맙)’(한국쿄와기린㈜)과 ▲황반변성 치료제인 ‘라니비주맙’ 제제에 대해 국내에서 두 번째*로 개발된 동등생물의약품(바이오시밀러)인 ‘루센비에스주10밀리그램/밀리리터(라니비주맙)’(㈜종근당)가 있다.국내 첫 번째 개발 바이오시밀러 품목: 삼성바이오에피스㈜의 ‘아멜리부주10밀리그램/밀리리터(라니비주맙, 유전자재조합)이다.
-> 2022년 11월 허가심사 결과 등 정보공개 현황