의약품의 품목허가․신고 이후 안전성․유효성을 지속 확보하고 품목의 효율적인 관리를 위해 5년마다 품목허가․신고를 갱신하는 이른바 의약품 품목갱신제도가 의약품의 주기적·체계적 품목허가 관리 수준을 높이고 있는 것으로 나타났다.
지난해 의약품 품목갱신을 통해 4,165품목이 정리,되었으며, 1,009품목이 허가변경 등 안전조치를 취했다. 연도별 갱신 대상 품목 현황은 (’18년) 4,798개(10%)를 시작으로 (’19년) 7,571개(27%) → (’20년) 8,083개(44%) → (’21년) 8,405개 63% → (’22년) 7,303개(78%) → (’23년 6월) 9,904개(100%)로 전품목의 검토가 가능할 전망이다.
의약품 품목갱신 제도는 2018년부터 본격 시행됐으며 이미 허가·신고된 의약품을 5년 주기(1주기: ’18∼’23)로 ▲안전성·유효성 등 안전관리자료 ▲품질관리자료 ▲표시기재자료 ▲제조·수입실적 등을 평가하는 제도다.
- 의약품 품목갱신 현황
식품의약품안전처(처장 김강립)는 17일 허가·신고된 의약품을 주기적이고 체계적으로 관리하기 위해 시행되고 있는 ‘의약품 품목갱신 제도’의 2021년 의약품 품목갱신 결과를 공개했다.2021년 의약품 품목갱신 결과에는 2018년 제도 시행 이후 지난 4년(’18~’21년)간의 의약품 품목갱신 결과도 함께 담았다.
식약처는 지난 4년간 품목갱신 검토 결과를 바탕으로 의약품의 안전한 사용 강화를 위한 허가사항 변경 명령과 안전성·유효성 재확인을 위한 임상 재평가 공고 등 안전조치를 취했다.
지난 4년간 ‘아스피린제제(진통제)’ 등 105개 성분(2,265개 품목)의 효능·효과, 용법·용량 개선 등 허가·신고사항 변경을 명령했고, ‘포르모테롤푸마르산염제제(기관지천식약)’ 등 총 9개 성분(66개 품목)에 대해서는 안전성·유효성의 재입증을 위한 임상재평가 실시를 공고했다.
특히 2021년에는 총 38개 성분(1,009개 품목)에 대해 허가·신고사항 변경을 명령했으며, 처음 3년간(’18∼‘20)의 총 67개 성분(1,256개 품목) 대비 큰 폭으로 증가한 수치다.
이는 의약품 품목갱신 제도 본격 운영 4년 차를 지나며 허가·신고된 의약품의 주기적·체계적 관리 수준이 향상되는 등 의약품 품목갱신 제도가 일정 수준 정착 단계에 도달한 결과로 분석된다.
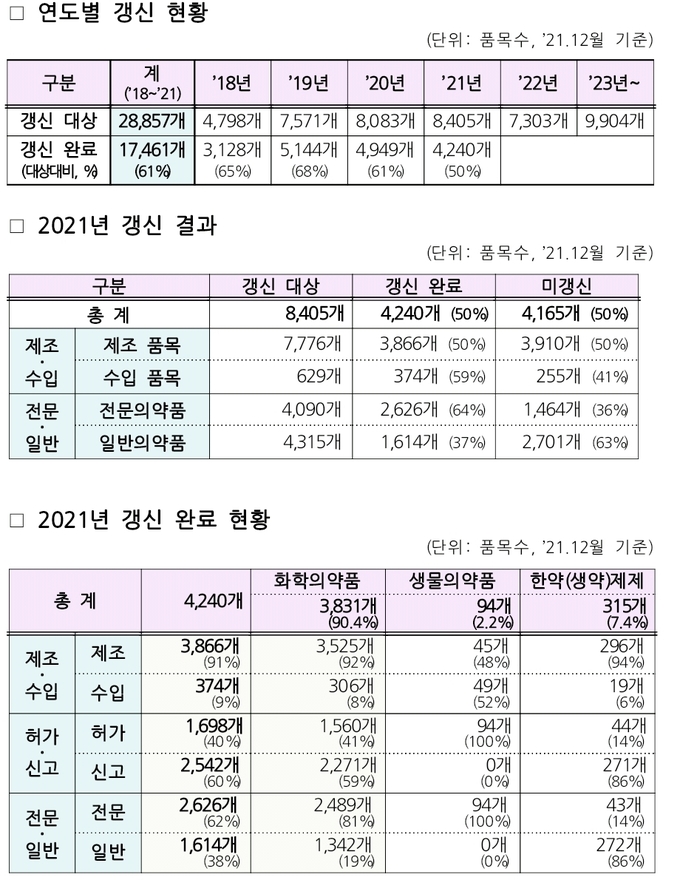
식약처는 의약품 품목갱신 1주기(’18∼’23) 대상 총 4만 6,064개 품목 중 4년(’18∼’21)동안 63%(2만 8,857개 품목, 누적)를 진행했다.
2021년까지 지난 4년간 품목갱신이 진행된 2만8,857개 품목 중 1만7,461개 품목(61%)의 갱신이 완료됐으나, 1만 1,396개 품목(39%)은 유효기간 만료 등으로 정리됐다.
2021년의 경우, 품목갱신 대상 8,405개 품목 중 4,240개(50%)품목은 갱신됐고, 4,165개(50%) 품목은 유효기간 만료 등으로 정리됐다.
식약처는 품목갱신 결과 공개가 업계의 의약품 품목갱신 제도에 대한 이해도를 향상시키고 제품 개발·출시를 위한 허가·신고 품목 현황을 파악하는 데 도움을 줄 수 있을 것으로 기대하고 있다.













