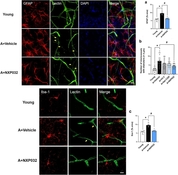
넥스모스(공동대표 심정욱, 조강준)는 넥스모스가 개발한 DNA압타머 복합체인 신물질 NXP032가 혈관성 치매 동물모델에서 손상된 신경혈관을 완화하여 인지기능 개선효능 관련 경희대학교 김연정 교수팀과의 공동 논문이 세계적인 과학저널 네이처(Nature) 자매지인 사이언티픽 리포츠(Scientific Reports) 최신호에 게재되었다고 2일 밝혔다. ‘NXP032 혈관성 치매 동물모델에서 손상된 신경혈관을 완화하여 인지기능 개선 효능 발견’(NXP032 ameliorates cognitive impairment by alleviating the neurovascular aging process in aged mouse brain, 26 May 2023) 제목으로 지난 5월26일자 최신호 사이언티픽 리포츠에 게재된 이번 연구는 혈관성 치매 동물 (마우스)모델에 NXP032를 직접 경구 투여하여 진행되었다는데 의미가 있다. 경희대 김연정 교수 연구팀은 기존 연구에서도 NXP032의 비타민C 항산화 기능 향상을 통해 노화 과정에서 발생하는 산화 스트레스의 효과적인 감소를 유도함으로써 인지장애 개선에 대한 가능성을 입증한 바 있다. 김연정 교수는 "현재 혈관성 치매
카이노스메드가 '2023 바이오 인터내셔널 컨벤션(BIO International Convention)'에 참가하여 KM-819의 기대감을 공유한다고 전했다 이번 컨퍼런스에서 카이노스메드는 자회사인 FAScinate와 함께 글로벌파마와 연구기관을 비롯해 여러 기관과 미팅을 갖고, 현재 미국과 한국에서 진행중인 파킨슨질환과 다계통위축증 임상 2상에 대해 설명하고 공동개발 등 차후 개발 계획에 대해 의논할 예정이다. 카이노스메드가 개발한 KM-819는 1) 신경세포 내 FAF1의 비정상적 활성 및 알파시누클레인 단백질의 비정상적 축적을 제거하여 도파민 신경세포를 보호하는 근본적 치료제인 first-in-class 약물이기 때문에 그동안의 약물들과는 다른 새로운 기전이라는 점과, 2) 파킨슨병 대상으로 미국 임상2상을 수행, 다계통 위축증 대상으로 한국 임상2상을 현재 수행하고 있는점, 3) 특히, 파킨슨병 대상의 미국 임상2상은 미국 자회사인 FAScinate가 글로벌 헬스케어 기업 로슈의 웨어러블 디지털 바이오마커 측정 디바이스를 접목한 프로토콜을 추진하고 있다는 점에서 다수 글로벌사 및 해외 기업들의 많은 관심을 받을 것으로 기대되고 있다.

오름테라퓨틱(대표 이승주)은 이번달 2일(현지시각)부터 5일간 미국 시카고에서 열리는 ASCO(미국임상종양학회)에서 ORM-5029의 임상 1상 시험에 대한 포스터를 게재한다고 2일 밝혔다. 이번 포스터 발표는 미국 임상이 진행 중인 캘리포니아대(UCLA) 데이비드 게펜 의과대학의 사라 허비츠(Sara A. Hurvitz) 교수(유방암 임상 연구 책임자)가 맡는다. 허비츠 교수는 ‘HER2 양성 유방암’ 항체-약물 접합체(ADC) ‘엔허투’(trastuzumab deruxtecan)와 1세대 HER2 ADC인 ‘캐싸일라’(trastuzumab emtansine)를 비교하는 DESTINY-Breast03 임상연구를 진행한 바 있다. 오름테라퓨틱은 ASCO에서 ‘HER2 발현 진행성 고형 종양 환자를 대상으로 HER2 표적 GSPT1 분해제인 ORM-5029에 대한 최초의 임상 1상 시험’의 디자인을 보여줄 예정이다. 지난해 10월, 첫 환자 투여가 시작된 이번 임상시험은 엔허투 등 기존 HER2 표적치료제에 재발하거나 불응하는 유방암 치료제 개발을 목표로, 유방암 환자 80여명을 대상으로 한다. 여기에는 UCLA를 비롯해, MD 앤더슨 암 센터(MD Ander

신약 개발 등 혁신 바이오 기술로 중무장한 국내 바이오 유망창업기업들이 6월 미국 보스톤에서 개최되는 글로벌 바이오 최대 행사인‘바이오USA’에 본격 진격해 글로벌 시장 공략에 나선다. 바이오분야 정부출연연구기관인 안전성평가연구소(소장 정은주)와 (사)한국엔젤투자협회 등은 6월 5일부터 8일까지(현지시각)까지 미국 보스톤에서 개최되는‘2023 바이오USA’행사에 국내 유망 바이오창업기업 45개사가 참여해 글로벌 사업화를 위한 전시 홍보 및 네크워킹, 파트너링에 나선다고 2일 밝혔다. 바이오USA는 미국생명공학협회(Biotechnology Innovation Organization)가 매년 주최하는 세계 최대 규모의 바이오산업컨퍼런스로, 올해 행사에는 전 세계 65개국, 8,000여개 이상의 제약·바이오 기업이 참여해 기술 소개 및 비즈니스 파트너링을 진행할 예정이다. 바이오USA는 해마다 국내 제약 등 바이오기업들이 글로벌 사업화를 위해 가장 많이 참여하는 국제 행사로, 이번 행사에 참여하는 초격차 프로젝트 참여기업 등 국내를 대표하는 유망 바이오스타트업 역시 현장 프리젠테이션 등을 통해 회사 보유 기술 및 파이프라인을 적극 홍보하고, 글로벌 대형 제약사들과

브릿지바이오테라퓨틱스(KOSDAQ 288330)는 다음 달 미국에서 개최되는 ‘2023 바이오 인터내셔널 컨벤션(이하 ‘바이오 USA’)’에서 최신 사업 진전 내용을 소개하는 ‘발표 기업(presenting company)’으로 선정됐다고 밝혔다. 바이오 USA는 60개 이상의 국가에서 1만 4천여 명의 제약∙바이오 산업 전문가들이 모여 혁신 신약 연구개발 성과를 공유하고 새로운 협력 기회를 모색하는 세계 최대 규모의 제약∙바이오 파트너링 행사로, 올해는 내달 5일부터 8일까지 나흘간 미국 보스턴에서 열린다. 브릿지바이오테라퓨틱스는 현지시간 6일 오후 3시 15분에 업계 관계자 및 잠재적 파트너사 등을 대상으로 기업 소개 발표를 진행한다. 파벨 프린세브(Pavel Printsev) 사업개발 디렉터는 이번 발표를 통해 혁신 신약을 중심으로 한 회사의 사업 비전을 비롯하여, 폐암과 폐섬유증 영역에서의 최신 연구개발 현황 및 전망을 소개하게 된다. 특히, 최근 혁신 진단 기술을 인수하며 본격화한 신규 사업에 대해 글로벌 무대를 대상으로 최초로 선보인다. 특히, 혁신적인 신약 과제 및 기술에 대한 수요가 어느 때보다 높은 상황에서 브릿지바이오테라퓨틱스는 글로벌 제약

미국 시장에 성공적으로 진입한 한미약품의 호중구감소증 치료 바이오신약 ‘롤론티스 프리필드 시린지주’의 차별화된 임상 근거가 지속적으로 축적되고 있다. 한미약품은 지난 19일 서울 소공동 롯데호텔에서 열린 2023 대한종양내과학회 위성 심포지엄(Satellite Symposium) 유방암 세션에서 한국인 및 아시아인 유방암 환자 대상의 임상 분석을 통해 롤론티스의 유효성과 안전성을 확인한 연구 결과가 발표됐다고 26일 밝혔다. 이번 연구는 미국 FDA의 롤론티스 시판허가 근거가 된 글로벌 임상 3상에 대한 통합 및 사후 분석 결과로, 분당차병원 혈액종양내과 문용화 교수가 관련 내용을 발표했다. 문 교수는 롤론티스 3상 임상에서 국내 최다 피험자를 등록해 연구를 주도하는 등 한국과 미국에서의 시판허가에 기여했다. 이 세션의 좌장은 고려대학교 구로병원 종양내과 박인혜 교수가 맡았다. 문 교수는 "항암치료 이후 발생할 수 있는 중증 호중구감소증의 기간(Duration of Severe Neutropenia, DSN) 및 호중구 수치의 회복 시간 등 다양한 평가지표에 대해 한국인, 아시아인을 포함한 모든 하위 집단에서 일관된 유효성을 확인했고, 전반적인 안전성 프로파
제넥신 (095700, 대표이사 닐 워마, 홍성준)은 자궁경부암 치료용 DNA백신 GX-188E(성분명: 티발리모진 테라플라스미드)와 림프구감소증 면역항암제 후보물질 GX-I7(지속형 인터루킨-7, 성분명: 에피넵타킨 알파), 키트루다®(KEYTRUDA®, 성분명: 펨브롤리주맙)의 삼중 병용 요법에 대한 두경부암(HNSCC, head and neck squamous cell carcinoma) 연구자 주도 임상 2상 초록이 ASCO 2023(미국임상종양학회 2023) 공개됐다고 26일 밝혔다. 이번 임상은 김혜련 연세대학교 세브란스병원 종양내과 교수 주도로, 고윤우 이비인후과 교수팀과 공동으로 진행한 연구자 주도 2상 임상 연구로, 수술을 앞둔 총 11명의 HPV양성 두경부암 환자들을 대상으로 키트루다 200㎎을 1일 및 22일차에 투약하고 GX-188E 2㎎을 1일, 8일, 22일, GX-I7을 수술 전인 8일차에 투약하는 수술 전 선행 보조요법(neoadjuvant)의 임상적 효용성을 평가했다. 일차평가변수로 주요 병리학적 반응(MPR, Major Pathological Response)과 이외에도 안전성과 재발율, 생존율 등을 평가했다. 이번에 공개된

한미약품의 이상지질혈증 치료 복합신약 ‘로수젯’이 고강도 스타틴 단독 요법 대비 임상적 유용성이 크다는 점을 확인한 연구 결과가 국제 학술지에 연속 등재되고 있다. 한미약품은 최근 세계적 국제학술지 란셋(The Lancet, IF : 202.731)의 자매지 ‘eClinicalMedicine’ (IF : 17.033)에 로수젯 레이싱 연구의 세번째 하위 분석 결과가 등재됐다고 25일 밝혔다. 로수젯을 이용한 대규모 임상인 ‘레이싱 연구’가 작년 7월 란셋에 등재된 이후, 첫번째 하위 분석 결과와 두번째 하위 분석 결과는 유럽심장저널(IF : 35.855)과 미국심장학회지(IF : 27.203)에 각각 등재된 바 있다. 이번에 등재된 세번째 하위 분석은 연세대학교 세브란스병원 심장내과 연구팀인 홍범기, 김중선, 이승준 교수와 영남대학교병원 순환기내과 박종일 교수 주도로 진행됐다. 이 연구에서는 스텐트 삽입술(경피적 관상동맥 중재술, percutaneous coronary intervention, PCI)을 받은 환자 중 로수젯 투여군이 고강도 스타틴 단일제 투여군 대비 심혈관 사건 발생에서는 차이가 없으며, LDL-C 목표 도달 및 내약성에서는 더 우수하다는

최근 IDMC(독립적 데이터 모니터링 위원회)로부터 NASH 치료제로의 개발을 중단없이 지속하라는 권고를 받은 한미약품의 LAPSTriple agonist(랩스트리플아고니스트, 국제일반명 : efocipegtrutide)가 적응증 확장을 통해 혁신 가능성을 확대하고 있다. 한미약품은 지난 19일부터 24일까지(현지시각) 미국 워싱턴DC에서 열린 미국흉부학회 국제 컨퍼런스 ‘ATS(American Thoracic Society) 2023’에서 LAPSTriple agonist를 특발성 폐 섬유증(idiopathic pulmonary fibrosis, IPF) 치료제로 개발할 수 있는 가능성을 확인한 연구 결과 1건을 포스터로 발표했다고 24일 밝혔다. LAPSTriple agonist는 체내 에너지 대사량을 증가시키는 글루카곤(Glucagon), 인슐린 분비 및 식욕 억제를 돕는 GLP-1, 인슐린 분비 촉진 및 항염증 작용을 하는 GIP 수용체를 동시에 활성화하는 삼중작용 바이오신약으로, 한미약품은 현재 글로벌 임상 2상을 통해 NASH 치료제로 개발중인 동시에 IPF 등 희귀질환 영역에서도 다양한 혁신 가능성을 탐색하고 있다. 이미 미국 FDA와 유럽 EM
한올바이오파마의 미국 파트너사 이뮤노반트(Immunovant)가 지난 22일(미국시간) 2022년 사업보고서를 통해 자가면역질환 치료제로 개발되고 있는 FcRn 항체신약 ‘바토클리맙’과 ‘IMVT-1402’에 대한 개발 현황을 발표했다. 한올바이오파마는 지난 2017년 이뮤노반트의 모회사인 로이반트(Roivant Sciences)에 자가면역질환 치료제 후보물질인 바토클리맙과 HL161ANS(이뮤노반트 프로젝트명: IMVT-1402)를 라이선스 아웃한 바 있다. 현재 바토클리맙과 HL161ANS는 다양한 자가면역질환에서 자가 투여가 가능한 피하주사 형태로 개발되고 있다. 이뮤노반트는 IMVT-1402의 안전성과 내약성, 그리고 약물 작용 효과(Pharmacodynamics, PD)를 평가하기 위한 임상 1상을 뉴질랜드에서 개시했다. IMVT-1402는 지난 동물 실험을 통해 바토클리맙과 비슷한 수준의 병원성 항체(pathogenic antibody) 감소 효과를 보이면서도 콜레스테롤 및 알부민 수치에 거의 영향을 주지 않은 것으로 나타나 계열 내 최고(best-in-class) 치료제가 될 수 있을 것으로 기대되고 있다. 이번 임상 1상은 IMVT-1402의